入試に役立つ理科実験「電池をつくる」
こんにちは。理科実験教室を担当している望月です。
今回の話は、教科書に出てくる「電池」の話です。

写真は、
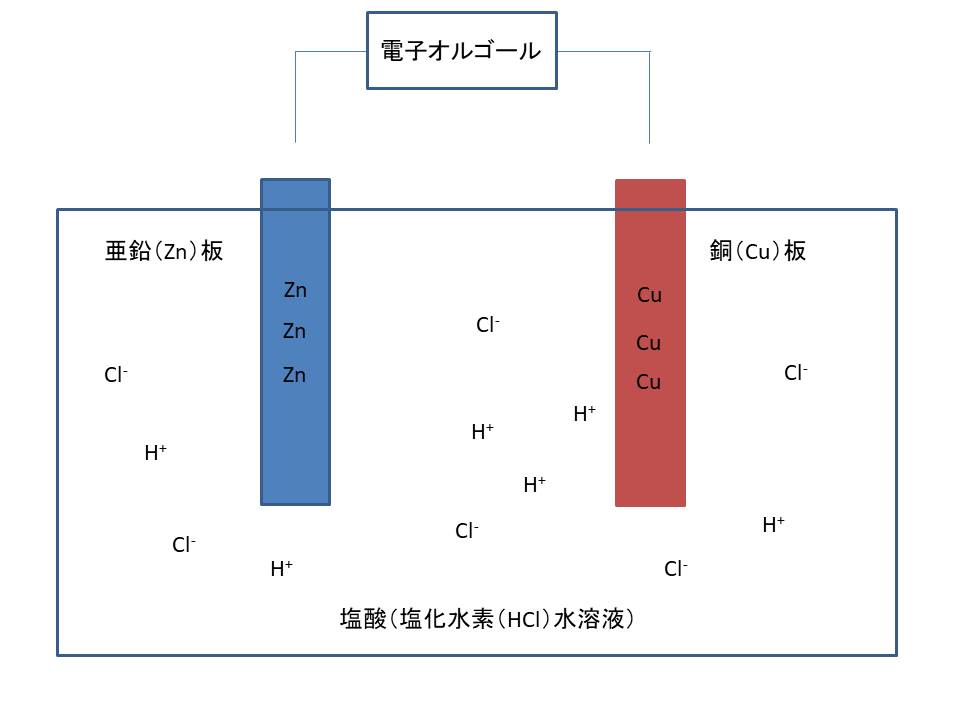
「ボルタ電池」をつくって、そこから発生する電流を使い、
電子オルゴールを鳴らしているところです。
透明な容器の中には、
・水溶液
・金属板
が入っています。
これだけでどうやって電流が発生するのでしょうか。

中に入っている金属の板は、実は2種類です。
・銅(Cu)板
・亜鉛(Zn)板
そして、中に入っているのは「薄い塩酸(HCl)」です。
塩化水素の水溶液である塩酸の中には、
・水素イオン(+イオン)
・塩化物イオン(-イオン)があります。
金属は、水にとけてイオンになりやすいものとなりにくいものがあり、
水素と比較して、
Zn > H > Cu となります。つまり、
亜鉛は水素や銅よりイオンになりやすい。
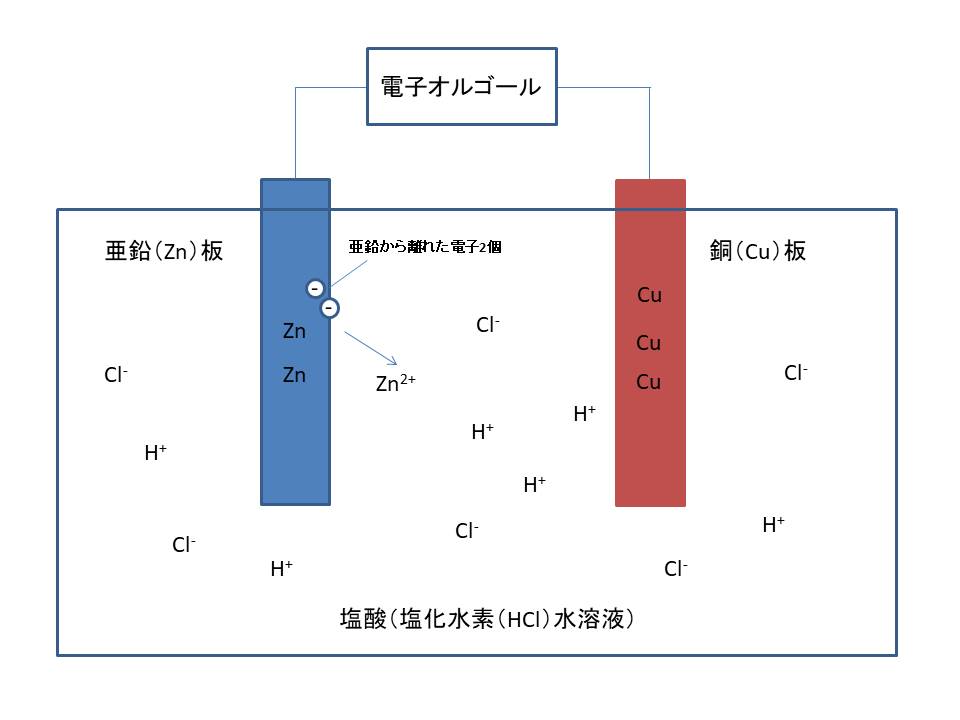
そのため、
亜鉛板が次第にとけてイオンになっていくとともに、水素はイオンではなくなっていく。
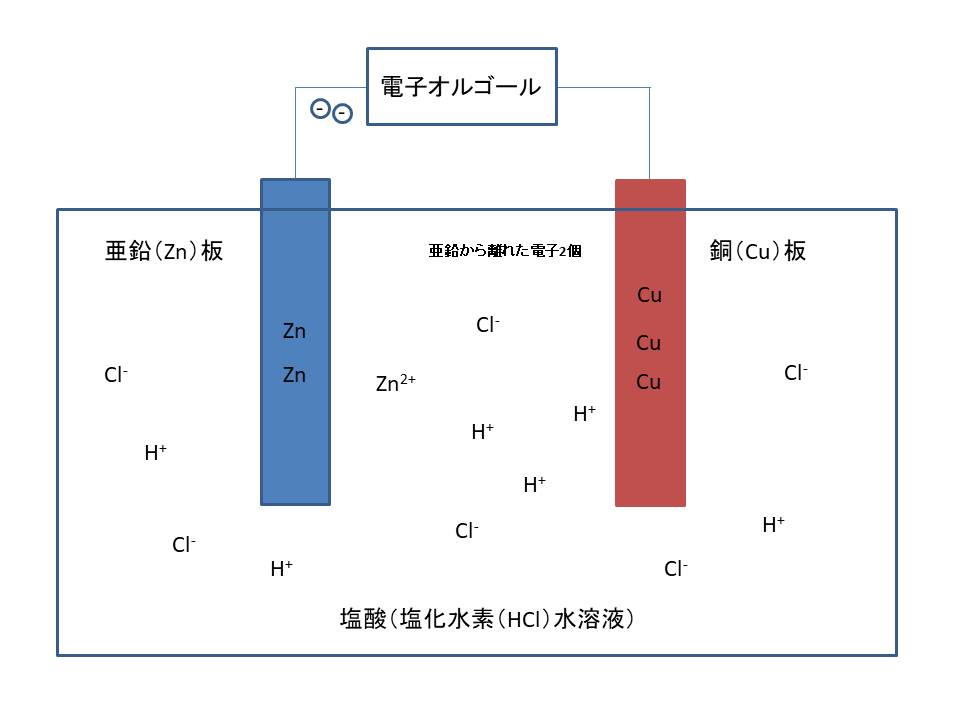
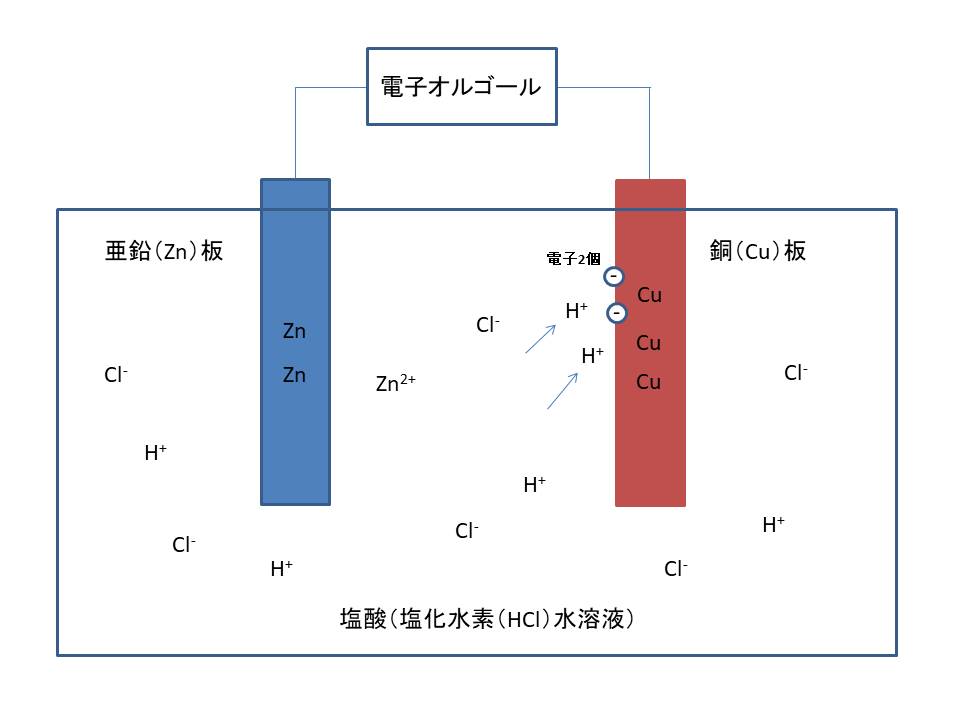
そのときに放した「電子」が導線→電子オルゴール→導線→銅板で、
水素イオンに与えられ、水素の泡が発生します。
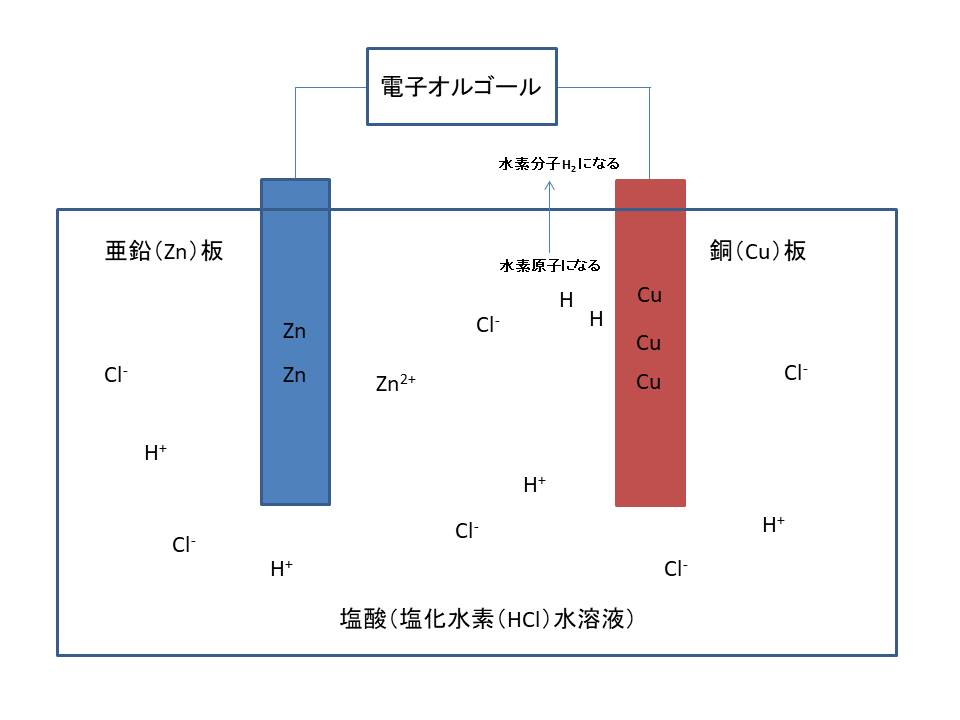 こうして、
こうして、
・亜鉛板が溶けていく。
・銅板の表面に水素の泡がつく。
現象とともに、電子オルゴールが鳴るのですね。
このように分割した図を書いてみるのもよいでしょう。










